
高通量mRNA/LNP筛选
抗体-LNP偶联包封服务
RNP-LNP包封
荧光标记LNP合成
常规服务

细胞转染试剂盒

应用试剂盒

器官靶向试剂盒

验证试剂盒

DNA试剂盒

蛋白试剂盒
“在探索心脏疾病治疗的新途径中,科学家们不断寻求创新方法以增强治疗效果并减少副作用。近期,一项关于使用脂质纳米颗粒(LNPs)递送改良mRNA(modRNA)至心脏的研究为这一领域带来了突破性的进展。今天,我们就来深入了解一下这项令人振奋的研究成果。”
1.1 LNP特性与组成:
本研究中测试的LNP制剂由C12–200离子化脂质、胆固醇、辅助脂质(DOPC或DOPE)和PEG缀合的脂质(DMG-PEG)组成。通过调整这些组分的摩尔百分比,我们制备了三种不同的LNP制剂。结果显示,这些制剂在粒径、电荷、多分散性和modRNA封装效率方面表现出相似性(图1)。

图一、不同成分LNP的表征
1.2 体外转染效率:
我们首先在体外评估了eGFP-modRNA LNP制剂在模拟心脏组织的细胞类型中的转染效率,包括人诱导多能干细胞衍生的心肌细胞(iPS-CMs)、永生化的人皮肤微血管内皮细胞(HMEC-1)、人诱导多能干细胞衍生的成纤维细胞(iPS-FBs)和心外膜衍生细胞(EPDCs)。通过流式细胞术和荧光显微镜测量eGFP表达水平,结果显示,所有细胞类型在用eGFP modRNA-LNP处理后均表现出比柠檬酸缓冲液中的modRNA更高的转染效率(图2)。在三种C12–200 LNP制剂中,C12–200 40%/Chol. 43.5%/DOPE 15% LNP在转染成纤维细胞和心外膜细胞方面最为高效。
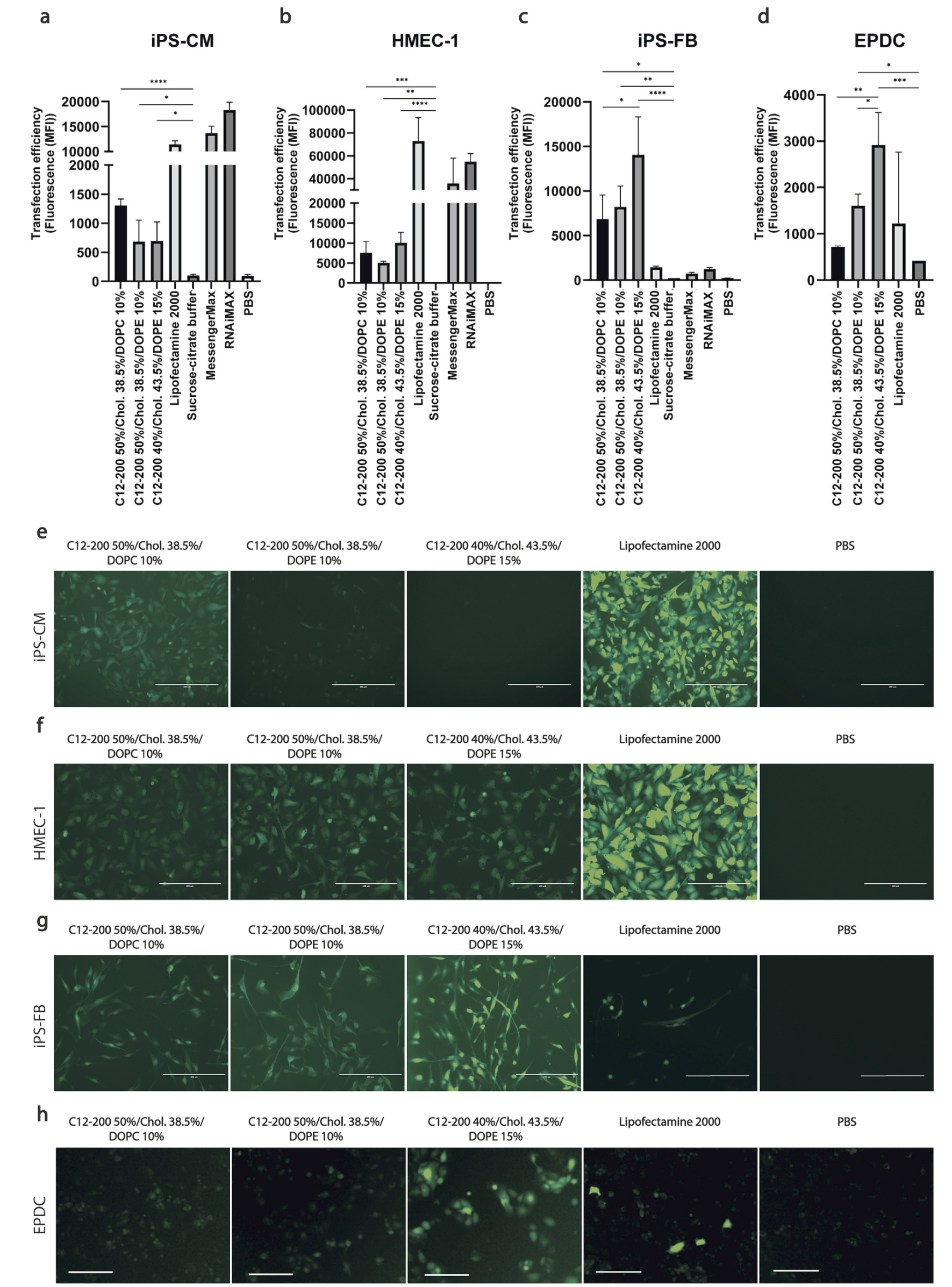
图一、不同成分LNP的体外细胞表达
1.3 体内转染效率:
接下来,我们在体内评估了所有LNP的递送效率。通过心肌内注射荧光素酶-modRNA LNP,并使用生物发光成像和组织裂解物分析来量化modRNA的翻译水平。结果显示,与柠檬酸缓冲液中的modRNA相比,LNP介导的modRNA递送在心脏组织中表现出更高的转染效率(图3)。此外,我们还检查了LNP在注射后24小时内的生物分布,发现LNP主要留在注射部位(左心室壁),而其他器官的LNP再分布水平相对较低(图3d和图S3)。

图三、不同成分LNP的体内表达

图四、不同处方LNP在心脏内细胞水平表达
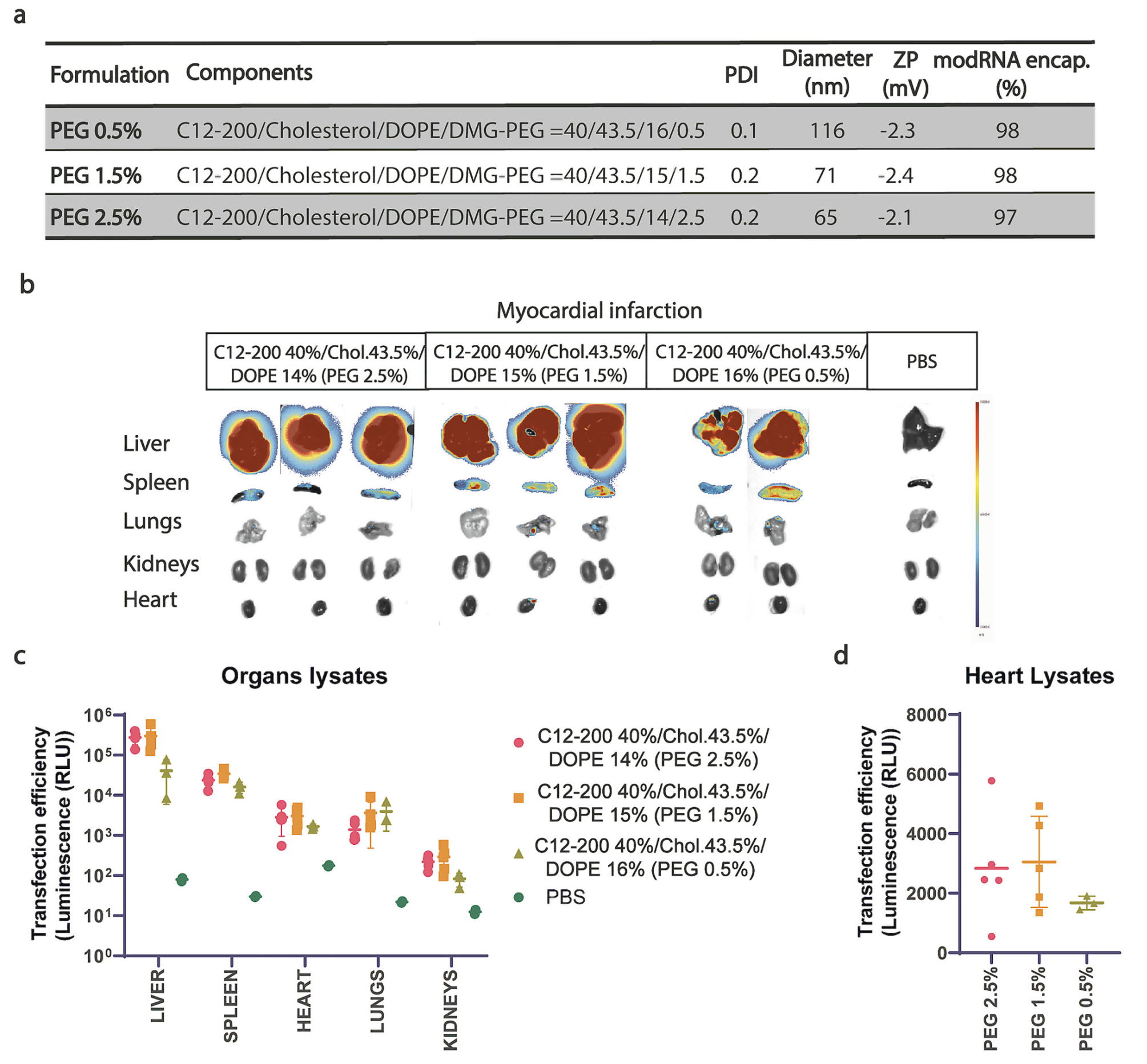
图五、不同PEG水平对心脏表达的影响
综上所述,本研究结果强调了LNPs作为心脏modRNA递送系统的潜力,其性能优于柠檬酸缓冲液中的modRNA。同时,进一步优化LNP制剂以提高其心脏特异性转染效率仍然是一个重要的研究方向。
参考文献:Labonia, M. C. I., et al. "Cardiac delivery of modified mRNA using lipid nanoparticles: Cellular targets and biodistribution after intramyocardial administration." Journal of Controlled Release 369 (2024): 734-745.
